La mesa es como una plataforma que se utiliza para organizar todos los elementos que se encuentran en la naturaleza, y algunos que son hechas por el hombre, incluso. Es útil porque organiza cada elemento en una caja, una especie de cómo organizar su cocina en especias picantes, especias dulces, azúcar y harina, por ejemplo. Así que cuando se quiere cocinar una tormenta, ya sabes dónde conseguir los ingredientes necesario- que se pueda imaginar la tabla periódica como lista de la naturaleza de los ingredientes. El aprendizaje de las propiedades de cada ingrediente y saber lo que sucede cuando se mezclan a ciertas concentraciones a temperaturas y presiones específicas es lo que hace un químico inorgánico.
La tabla periódica se puede utilizar para determinar las siguientes propiedades de los materiales:
Número atómico (Z): Elementos están organizados de acuerdo a su número atómico y dispuestos en orden de números atómicos bajos a altos números atómicos. El número atómico en sí también se puede decir mucho sobre la element- puede ayudar a entender la valencia, el número de coordinación, y la posición que usted esperaría encontrar en la tabla periódica. Números atómicos varían de 1 a 118. El número atómico representa el número de protones que existen en el núcleo.
Número de protones: El protón constituye una parte del núcleo. Es una partícula con carga positiva que está contrarrestado por los electrones, pero los electrones orbitan alrededor del exterior en su lugar. El número de protones puede determinar el número de electrones puede orbitar alrededor del átomo-esto, a su vez, afecta a la reactividad y la química del átomo.
Reactividad: La reactividad de los elementos aumenta de izquierda a derecha en la tabla periódica. Cada elemento que va de izquierda a derecha tiende a ser más reactiva. Pero, a la derecha el momento son los gases nobles, y son casi completamente inerte. La reactividad todos aumenta a medida que bajan la tabla periódica, por ejemplo rubidio es mucho más reactivo que el sodio.
Electronegatividad: Esta propiedad determina la cantidad del elemento atrae electrones. Esto también es una buena medida de la reactividad, ya que cuanto más que un elemento atrae electrones, el más reactivo es. El elemento más electronegativo sobre la mesa es el flúor. Los aumentos de electronegatividad que van de izquierda a derecha, y disminuye bajando la mesa.
Masa: A medida que avanza de izquierda a derecha y de arriba a abajo, que siempre está agregando más protones en el átomo. Esto tiene la tendencia general para que los elementos posteriores más pesado que los elementos anteriores. Pero usted debe darse cuenta de que esto es sólo una tendencia general, y hay algunas excepciones a la regla.
Densidad: Como usted va abajo de la mesa, la densidad del átomo increases- al ir de izquierda a derecha, la densidad también aumenta.
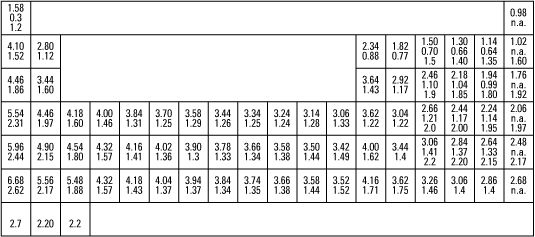
Traslado de izquierda a derecha en la tabla periódica se muestra en la siguiente figura, el tamaño atómico disminuye debido a la carga nuclear adicional debido a la adición de neutrones y protones en el núcleo. Esto hace que los electrones orbitales estar más estrechamente vinculados, y los aumentos de energía de ionización debido a eso.
La tabla periódica.
Maravillas Modernas Debido a Química Inorgánica
Desde los albores de la humanidad, los materiales han desempeñado un papel fundamental para nuestra existencia. La capacidad de hacer vivienda para defenderse de tiempo y húmedos malas condiciones, por ejemplo, sin duda hizo que viven mucho más fácil, pero hoy en día este tipo de apoyos elementales son considerados como partes discontinuas de nuestra vida cotidiana. Los materiales que utilizamos hoy en día son muy diferentes de lo que hemos utilizado en el pasado. Tres elementos - carbono, aluminio y silicio - han ayudado al proceso de modernización. Hay muchos más elementos que han jugado su parte, por supuesto, pero estos tres son indiscutibles.
El carbono es un elemento versátil y puede ser mezclado con muchos otros materiales para hacer materiales compuestos y aleaciones. El carbono es uno de los elementos más prolíficos en la mesa- periódica que es la materia de la vida, la columna vertebral del ADN, y una piedra angular de la sociedad moderna. Son posibles todos los grandes edificios grandes que ves a tu alrededor en las ciudades de hoy en día debido al carbono. Metal que se refuerza y aleado con carbono es a menudo fuerte y ligero, por lo que es más fácil de usar y de mayor duración. Grafeno, fullerenos, y nanotubos de carbono muestran una gran promesa para un futuro uso como aditivos para reforzar materiales, lo que hace aún más resistentes al desgaste y de mayor duración, al tiempo que reduce el peso, también. A medida que aprenda más acerca de este elemento puede estar seguro de encontrar en más y más aparatos cotidianos a medida que avanzamos en el tiempo.
El aluminio, por otra parte, es un lugar nuevo material. No fue sino hasta hace poco que el aluminio podría incluso ser aislado de su forma de óxido muy estable y más común. Pero desde entonces se ha convertido en la salida al material para una serie de aplicaciones. En cuanto a los vuelos espaciales, hay un dicho: Si usted desea hacer una nave espacial que puede recoger cualquier material que desee, siempre y cuando sea de aluminio. Ha sido probado y comprobado hasta el punto de que es difícil de reemplazar en esta etapa, pero al final es probable que sea reemplazado por materiales compuestos que están hechos de carbono. Pero mientras tanto no tomaría mucho tiempo para encontrar ejemplos de aluminio en su experiencia cotidiana - que puede encontrar en trenes, aviones y automóviles, y en las cocinas, loncheras, y todo tipo de aparatos porque es un durable, fuerte , y el material impermeable ligero.
El silicio es el elemento más estudiado en el planeta- hay una industria de miles de millones de dólares que está corroborada por las propiedades de este elemento. Es un semiconductor que tiene el potencial, cuando dopado, para ser más conductora, o menos conductora. Esta propiedad le da la capacidad de silicio para su uso en materiales y dispositivos para hacer 1s y 0s que traducen el código de computadora en impulsos eléctricos. Junto con el hecho de que el silicio es uno de los elementos más abundantes en el planeta, que está dispuesto a ser utilizado en el futuro inmediato, tal vez nunca pasan de moda. La edad de la tecnología de la información podría haber sido posible sin el silicio, pero puede haber tomado mucho más tiempo y no ser tan importante hoy como lo es.
El descubrimiento del oxígeno
El oxígeno fue descubierto por el químico sueco Carl Wilhelm Scheele en 1772. Él descubrió que calentando el óxido de mercurio, un gas (más tarde identificado como oxígeno) formado. Scheele llamó el "aire de fuego" de gas, ya que produce chispas, ya que entró en contacto con el polvo de carbón caliente.
Esta historia comienza con Platón y sus ideas sobre la naturaleza de la materia. Platón fue un filósofo griego que sugiere que toda la materia estaba hecha de cuatro elementos esenciales - fuego, aire, tierra y agua. Esta idea crudo duró varios siglos, casi sin oposición, y dio lugar a la teoría del flogisto, que en griego antiguo significa "quemar".
La principal precepto de la teoría del flogisto era que el fuego era en sí misma un elemento, por lo que en el momento cuando algo quemado, las llamas fueron consideradas pruebas de que el fuego (como elemento) estaba siendo separado del material. Esta era la creencia popular hasta el experimento de Scheele llevó químico francés Antoine-Laurent de Lavoisier de probar, en 1779, que cuando fue aislado de oxígeno, el fuego podría ser visto como una consecuencia de una reacción química, en lugar de como un elemento en la reacción. Fue Lavoisier quien dio nombre del elemento, oxígeno.
Por tirar la teoría del flogisto, Lavoisier abrió el camino para la química moderna. Eso hizo que los cambios dramáticos en la ciencia a partir de entonces, y fue debido en gran parte al descubrimiento del oxígeno.
El descubrimiento del helio
Tras su descubrimiento por el astrónomo francés Pierre Janssen JC en 1868, se pensaba que el helio de existir en el sol, pero no aquí en la tierra. Como él estaba observando un eclipse solar en la India, Janssen dio cuenta de una línea espectral amarillo brillante.
El sol brilla todos los días. Independientemente de qué tan lejos al norte o sur se vive en este planeta, el sol aún puede llegar a usted. El sol es una gran bola de fuego de varios millones de millas de distancia. De hecho, es un gran reactor nuclear, lleno de explosiones que hacen que la energía que se criticó a distancia y se emite en todas direcciones.
La luz que se ve desde el sol viene de todos los fotones se envían al espacio desde el sol, y el color de la luz se puede utilizar para determinar qué elementos están presentes gracias a nuestra comprensión de los niveles de energía de electrones y espectroscopia atómica. En resumen, la teoría es la siguiente. . . electrones orbitan alrededor de un átomo que tiene tantos electrones como está permitido para ese átomo.
Cada electrón tiene un cierto nivel de energía discreta, y cuando se excita el electrón se puede ver los niveles de energía usando un prisma, por ejemplo. Un prisma divide iluminación blanca que se ralentiza debido a la difracción, y se puede obtener toda la gama del arco iris de la luz blanca. Sin embargo, algunas fuentes de luz blanca faltan algunas bandas del arco iris colores-esto depende de la fuente de la luz. Las bandas que faltan acto como las huellas dactilares de los elementos químicos, y estas "huellas digitales" son únicos, así que usted puede utilizar para identificar los elementos, incluso si están muy lejos como las estrellas y otros planetas. Fue mirando el sol con una configuración tal que el helio fue descubierto primero.
La luz del sol tenía vendas en los mismos que se componen de un material desconocido, como nada de lo que había sido analizado en la tierra todavía. Fue nombrado después de que el sol, Helios. El descubridor Pierre JC Janssen tuvo que viajar a la India para hacer su observación durante un eclipse solar en 1868. Pero más tarde se descubrió que el helio está presente en la Tierra, y sin embargo, más tarde se descubrió entre los minerales de uranio. Simplemente va a demostrar que usted no tiene que ir todo el camino hacia el sol para encontrar su respuesta - es probablemente aquí entre nosotros ya. Sólo tienes que aprender a mirar de la manera correcta.
Importantes Términos Química
Hay muchas palabras y términos que son específicos de la química, la química inorgánica en este caso. Aquí está una lista de algunos de los términos más comunes y más interesantes que usted necesita saber.
Ciclo de Born-Haber: Un cálculo termodinámico importante que se utiliza para cuantificar la energía involucrada en la fabricación de compuestos iónicos.enlace covalente: El intercambio de electrones entre átomos, enlaces covalentes son normalmente bastante fuerte. Pueden ser enlaces simples, dobles o triples. Los enlaces covalentes tienen direccionalidad.La regla de Fajan: Se utiliza para determinar cualitativamente el grado de unión covalente en materiales iónicos. Los cationes experimentan mayor carácter covalente de acuerdo con el aumento de densidad de carga. En aniones, el grado de unión covalente aumenta al aumentar la polarizabilidad del ion.La ley de Hess: Para cualquier reacción química dada, la energía total requerida para completar la reacción es la misma sin importar el número de pasos necesarios para completar la reacción. Forma el conocimiento básico necesario para completar un cálculo utilizando el ciclo de Born-Haber. híbrido: Se utiliza para describir la mezcla de orbitales moleculares (s, p, d, f) de tal manera que se hibridan para formar equivalente pares solitarios y parejas de unión orbitales. sp hibridado orbitales son comunes para muchos compuestos de carbono orgánico.enlace iónico: Un enlace iónico se forma cuando hay una transferencia de electrones de un átomo a otro átomo. Se basa en las interacciones electrostáticas o columbic. cinética: Un estudio de la velocidad de una reacción. Está afectada por condiciones tales como la temperatura, la concentración, y el uso de un catalizador. Estructura de Lewis: Representación estructural de cómo se encuentran los electrones de valencia de una molécula o átomo, se utiliza para mostrar la presencia de pares de unión y no de unión pares solitarios.estado de oxidación: También conocido como el número de oxidación, una medida de la cantidad de electrones de un átomo tiene que convertirse en una especie neutra. Los electrones se pueden agregar o quitar para llegado el átomo neutro. En una reacción química si el número de oxidación aumenta, se reduce el elemento. tabla periodica: Una tabla de los elementos que están ordenados de acuerdo con un incremento sucesivo en el número atómico. efectos de resonancia: Se utiliza para describir la situación en la que una especie química dona o se retira electrones a través de solapamiento orbital con vecinos enlaces pi. En los procesos de resonancia, los electrones están deslocalizados y la energía de los electrones se estabilizan. control termodinámico: Las reacciones que crean productos con la energía más baja y el producto más estable se dice que están controlados por la termodinámica. No todas las reacciones crean el producto- más termodinámico algunos son controlados por la cinética de su lugar.valencia: Una medida del número de los electrones en la capa de valencia de un átomo. Destaca la capacidad de un átomo para experimentar una reacción, pero se usa con menos frecuencia en comparación con el número de oxidación.