Un ejemplo problema mecanismo de química orgánica
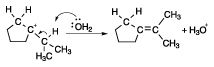
Supongamos que está trabajando una misión química orgánica, y se le pide que proponga un mecanismo para la conversión del alcohol muestra en la siguiente figura para el alqueno se muestra en la misma figura.
En primer lugar, desea identificar qué tipo de mecanismo que está tratando. ¿Es un mecanismo de base ácida o? Es un nucleófilo o un mecanismo electrófilo? ¿Es un mecanismo de radicales libres? Debido a que el reactivo es ácido sulfúrico (H2SO4) Más # 8710- (un símbolo que indica que la mezcla de reacción se calienta), la reacción será una reacción ácida.
En segundo lugar, identificar dónde va en el mecanismo. La conversión de un alcohol en un alqueno por lo general implica la deshidratación (pérdida de agua). Pero usted puede notar que el alqueno en el producto se encuentra en una posición inusual, ya que la deshidratación por lo general pone el alqueno adyacente al alcohol de partida. El producto en este caso tiene el doble enlace un átomo de carbono más lejos de su posición esperada. Por lo tanto, se podría esperar algo inusual en este mecanismo que explica la regioquímica inusual de la reacción.
Ahora que usted sabe aproximadamente donde vas en este mecanismo, puede comenzar a proponer una ruta para llegar allí. En un mecanismo de ácido, lo primero que desea buscar es un sitio en la molécula que puede ser protonado. El único sitio básico en el material de partida en este caso es el alcohol, por lo que el primer paso sería la protonación del grupo alcohol por el ácido sulfúrico.
El primer paso en mecanismos de ácido es casi siempre la protonación.
Como siempre, siga las convenciones para la flecha empujando, dibujo flechas de pleno encabezado de electrones a dónde van. (Los únicos mecanismos que utilizan flechas monoparentales son mecanismos de radicales libres.)
Debido a que muchos profesores de la química orgánica están convencidos de que el círculo más interno del infierno de Dante está reservado para aquellos estudiantes que obtienen consistentemente protonación de forma incorrecta, asegúrese siempre dibujar la flecha de los electrones en la base para el protón ácido que los electrones están atacando. Nunca cometer el pecado imperdonable de dibujar una flecha de un H + ácido. Además, para hacer siguiendo el movimiento de los átomos y los cargos más fáciles, los átomos en las partes de la molécula de que el cambio en la reacción se extraen de forma explícita con la estructura completa Lewis, como se muestra en la siguiente figura.
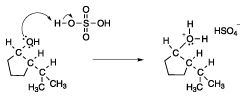
A continuación, examinar las consecuencias de la protonación. ¿Qué puedes hacer ahora que no podía hacer antes? Una cosa que puedes hacer ahora que el alcohol es protonado es formar un carbocatión. Aunque ion hidróxido, OH-, es un grupo saliente malo (bases fuertes son grupos salientes malos), el agua es un buen grupo saliente. Así, como en un mecanismo típico de la deshidratación de alcohol, el siguiente paso implica la pérdida de agua para crear un carbocatión secundario, como se muestra en la siguiente figura.
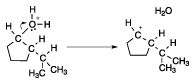
En la deshidratación de alcohol, cuando se forma el carbocatión, el siguiente paso es por lo general la formación del doble enlace mediante la eliminación de un protón. Si lo hace, en este paso, sin embargo, sería formar el doble enlace en la posición incorrecta. De alguna manera, el carbocatión necesita moverse de manera que cuando el hidrógeno se elimina, se forma el doble enlace en la posición correcta.
En una inspección más cercana, puede observar que el carbocatión se encuentra junto a un centro de carbono terciario. El carbocatión es actualmente un carbocatión secundario, pero que mal quiere convertirse en un carbocatión terciario. (Carbocationes terciarios son más estables que los carbocationes secundarios.) Un proceso de pensamiento más pragmático podría ser que aquí es donde el catión debe trasladarse a fin de conseguir la eliminación en el lugar correcto. Para obtener el carbocatión en la posición superior, se realiza un cambio de hidruro, que mueve el átomo de hidrógeno terciario y ambos de los electrones en el enlace CH al centro catiónico, dejando el carbono terciario con la carga positiva. Este paso se muestra en la siguiente figura.
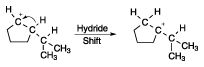
Ahora, la eliminación de un protón conduce a la alqueno correcta. La desprotonación se muestra en la siguiente figura, el uso de agua para regenerar una molécula de ácido. También puede utilizar la base conjugada del ácido sulfúrico como base aquí.