Los enlaces covalentes: tipos de fórmulas químicas
Hay varios tipos de fórmulas químicas que se pueden utilizar para representar los enlaces químicos. Estos incluyen fórmulas empíricas, molecular (o cierto
Conteúdo
Se puede predecir la fórmula de un compuesto iónico basado en la pérdida y ganancia de electrones, para llegar a una configuración de gas noble. Sin embargo, usted realmente no puede hacer ese tipo de predicción con compuestos covalentes, ya que se pueden combinar de muchas maneras, y muchos diferentes compuestos covalentes posibles puede resultar.
La mayoría de las veces, usted tiene que saber la fórmula de la molécula que estás estudiando. Pero usted puede tener diferentes tipos de fórmulas, y cada uno da una cantidad ligeramente diferente de la información.
Fórmula empírica: Sólo los elementos
los formula empírica indica los diferentes tipos de elementos en una molécula y la relación de número entero más bajo de cada tipo de átomo en la molécula. Por ejemplo, suponga que tiene un compuesto con la fórmula empírica:
Tres tipos diferentes de átomos están en el compuesto, C, H y O, y que están en la proporción más baja de todo el número de 2 a 6 C H 1 O. Así que la fórmula actual (llamado fórmula molecular o verdadera formula) puede ser cualquiera de los siguientes, u otro múltiplo de 2: 6: 1.
Molecular o verdadera fórmula: Dentro de los números
los fórmula molecular, o verdadera fórmula, le indica los tipos de átomos en el compuesto y el número real de cada átomo.
Usted puede determinar, por ejemplo, que la siguiente fórmula empírica es en realidad la fórmula molecular, también, lo que significa que en realidad hay dos átomos de carbono, seis átomos de hidrógeno y un átomo de oxígeno en el compuesto:
Para los compuestos iónicos, esta fórmula es suficiente para identificar plenamente el compuesto, pero no es suficiente para identificar compuestos covalentes. Para escribir una fórmula que representa el compuesto exacto que tiene en mente, a menudo se debe escribir la fórmula estructural en lugar de la fórmula molecular.
Fórmula estructural: Agregue el patrón de unión
La fórmula estructural muestra los elementos en el compuesto, el número exacto de cada átomo en el compuesto, y el patrón de unión para el compuesto. La fórmula de electrones punto y fórmula Lewis son ejemplos de fórmulas estructurales.
Mira las fórmulas de Lewis que se presentan en la siguiente figura.
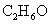
Ambos compuestos en la figura tienen dos átomos de carbono, seis átomos de hidrógeno, y un átomo de oxígeno. La diferencia está en la forma en que los átomos están unidos, o lo que unido a lo. Se trata de dos compuestos completamente diferentes con dos juegos completamente diferentes de propiedades:
La fórmula de la izquierda representa dimetil éter. Este compuesto se utiliza en algunas unidades de refrigeración y es altamente inflamable.
La fórmula de la derecha representa alcohol etílico, la variedad consumo de alcohol.
Simplemente saber la fórmula molecular no es suficiente para distinguir entre los dos compuestos.
Los compuestos que tienen la misma fórmula molecular pero diferentes estructuras se denominan isómeros el uno del otro. Para identificar el exacto compuesto covalente, necesita su fórmula estructural.





