¿Cómo distinguir electrolitos de no electrólitos
Los electrolitos son sustancias que conducen la electricidad en el estado fundido o cuando se disuelve en agua. No electrolitos son sustancias que no conducen la electricidad cuando en estos estados.
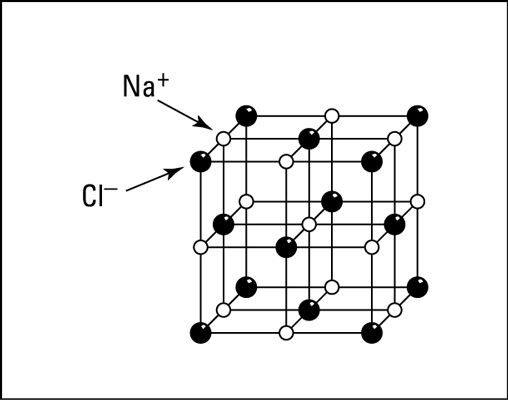
Cuando un compuesto iónico, tal como cloruro de sodio se pone en agua, las moléculas de agua se atraen tanto los cationes y aniones en el cristal y tirar de ellos en la solución (véase el cristal se muestra en la figura). Los cationes y aniones se distribuyen en toda la solución.
Puede detectar la presencia de estos iones mediante el uso de un instrumento llamado probador de conductividad. A las pruebas de conductividad probador si soluciones acuosas de diversas sustancias conducen la electricidad. Se compone de una bombilla con dos electrodos conectados.
La bombilla está enchufado a una toma de corriente, pero no se enciende hasta que algún tipo de conductor (sustancia capaz de transmitir electricidad) entre los electrodos completa el circuito. (Un dedo completará el circuito, por lo que este experimento debe ser hecho con cuidado.)
Al colocar los electrodos en agua pura, no pasa nada, porque no hay conductor entre los electrodos. El agua pura es un no conductor. Pero si usted pone los electrodos en la solución de NaCl, se enciende la bombilla de luz, debido a que los iones conducen la electricidad (llevan los electrones) de un electrodo a otro.
Usted ni siquiera necesita el agua. Si se va a derretir pura de NaCl (se requiere una gran cantidad de calor!) Y luego colocar los electrodos en el mismo, que iba a encontrar que la sal de mesa fundida también conduce la electricidad. En el estado fundido, los iones de NaCl son libres de moverse y llevar electrones, tal como son en la solución de agua salada.
Los científicos pueden obtener algunas buenas pistas sobre el tipo de enlace en un compuesto de descubrir si una sustancia es un electrolito o un no electrólito. Sustancias iónicamente unidos actúan como electrolitos. Pero unido covalentemente compuestos, en los que no hay iones están presentes, son comúnmente no electrólitos.
El azúcar de mesa o sacarosa, es un buen ejemplo de un no electrólito. Puede disolver el azúcar en el agua o fundirlo, pero no tendrá la conductividad. No hay iones están presentes para transferir los electrones.






