La identificación de objetivos, objetivos, hipótesis y variables para un estudio clínico
los objetivos o metas de un estudio son declaraciones generales cortos (a menudo sólo una declaración) de la finalidad general de la prueba. Por ejemplo, el objetivo de un estudio puede ser "para evaluar la seguridad y eficacia del fármaco XYZ en pacientes con hiperlipidemia moderado".
los objetivos son mucho más específicos que los objetivos. Objetivos generalmente se refieren al efecto del producto sobre las variables de eficacia y seguridad específicos, en puntos específicos en el tiempo, en grupos específicos de las materias. Un estudio de eficacia puede tener muchos objetivos de eficacia individuales, así como uno o dos de seguridad objetivos- un estudio de seguridad pueden o pueden no tener objetivos de eficacia.
Usted debe identificar uno o dos objetivos primarios - los que están más directamente relacionados con el objetivo del estudio y determinar si el producto pasa o no en el estudio. A continuación, puede identificar hasta varias decenas objetivos secundarios, que podrá incluir varias variables o las mismas variables en diferentes momentos o en diferentes subgrupos de la población estudiada.
Usted también puede mostrar un conjunto de objetivos exploratorios, que son menos importantes, pero todavía interesante. Por último, usted enumera una o más objetivos de seguridad (si se trata de un estudio de eficacia) o algunos de los objetivos de eficacia (si se trata de un estudio de seguridad).
Un conjunto típico de primaria, secundaria, exploratoria, y los objetivos de seguridad (este ejemplo muestra una de cada tipo) para un estudio de eficacia podría tener este aspecto:
Objetivo de eficacia primario: Para comparar el efecto de la droga XYZ, en relación con el placebo, en los cambios en el colesterol sérico total desde el inicio hasta la semana 12, en pacientes con hiperlipidemia moderada.
Objetivo de eficacia secundario: Para comparar el efecto del fármaco XYZ, en relación con el placebo, en los cambios en suero de colesterol y triglicéridos totales en suero desde el inicio hasta semanas 4 y 8, en los pacientes con hiperlipidemia moderada.
Exploratorio objetivo de eficacia: Para comparar el efecto de la droga XYZ, en relación con el placebo, en los cambios en los lípidos séricos desde el inicio hasta las semanas 4, 8 y 12, en subconjuntos masculinos y femeninos de los pacientes con hiperlipidemia moderada.
Objetivo de seguridad: Para evaluar la seguridad de la droga XYZ, en relación con el placebo, en cuanto a la ocurrencia de eventos adversos, cambios desde el inicio en los signos vitales (presión arterial y frecuencia cardíaca), y los resultados de laboratorio de seguridad (química, hematología, y así sucesivamente), en pacientes con hiperlipidemia moderada.
Hipótesis por lo general corresponden a los objetivos, pero están redactados de una manera que se relaciona directamente con la prueba estadística a realizar. Así que el objetivo principal precedente puede corresponder a la siguiente hipótesis: "La reducción media de 12 semanas en el colesterol total será mayor en el grupo de XYZ que en el grupo placebo."
Alternativamente, la hipótesis puede ser expresado en una notación matemática más formal y como un par nula y alternativa:
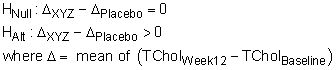
La identificación de las variables para recoger en su estudio debe ser sencillo después de haber enumerado todos los objetivos. En general, usted debe planear en la recogida de todos o algunos de los siguientes tipos de datos:
Información demográfica básica (como la fecha de nacimiento, género, raza y etnia)
Información sobre la participación del sujeto en el estudio (por ejemplo, la fecha de inscripción, si el sujeto se conocieron inclusión y criterio de exclusión, la fecha de cada visita, las medidas de cumplimiento y el estado final (completa, se retiró, perdió durante el seguimiento, y En Poco Tiempo)
Mediciones de referencia básicos (altura, peso, signos vitales, pruebas de laboratorio de seguridad, etc.)
El sujeto y el historial médico de la familia, incluyendo enfermedades, hospitalizaciones, tabaquismo y otras sustancias, y los medicamentos actuales y pasados
De laboratorio y otras pruebas (ECG, radiografías, etc.) los resultados relacionados con los objetivos del estudio
Las respuestas de los cuestionarios y otras evaluaciones subjetivas
La ocurrencia de eventos adversos
Parte de esta información debe registrarse una sola vez (como fecha de nacimiento, sexo y antecedentes familiares) - otra información (como los signos vitales, la dosificación y resultados de pruebas) pueden ser adquiridos en las visitas programadas o no programadas, y algunos pueden ser registrados solamente en momentos impredecibles, en todo caso (como eventos adversos).
Para los estudios muy simples, usted puede ser capaz de registrar todos sus datos en una sola (aunque grande) hoja de papel rayado, con una fila para cada tema y una columna para cada variable. Pero en los estudios clínicos formales, es necesario diseñar un Caso Formulario de Informe (CRF). Una CRF es a menudo un folleto o carpeta con una página para los datos de una sola vez y un conjunto de páginas idénticas para cada tipo de datos recurrentes.
Muchos excelentes plantillas de CRF se pueden descargar de la web (o simplemente entrar en "plantillas de CRF" en su navegador).

